ę╗ĪóŲ¾śI║åĮķ
╬õØhÉ█├±ųŲ╦ÄėąŽ▐╣½╦Š│╔┴óė┌1969─Ļ10į┬Ż¼Ū░╔Ē×ķųąć°╚╦├±ĮŌĘ┼▄Ŗ┐š▄Ŗ└ū▀_īWį║Ą─Ž┬ī┘Ų¾śI——╬õØhÉ█├±ųŲ╦ÄÅSĪŻ2006─Ļ▄ŖĻĀ═Ż▐kĖ─ųŲ×ķ├±ĀIėąŽ▐ž¤╚╬╣½╦ŠĪŻ╩Ūę╗╝ę╝»čą░lĪó╔·«aĪóõN╩█ė┌ę╗¾wĄ─ć°╝ę╝ēĖ▀ą┬╝╝ągŲ¾śIŻ¼╩Ū║■▒▒╩Ī╔·╬’«aśI░lš╣ęÄäØŻ©2008-2015Ż®Ż©Č§š■▐k░lĪŠ2008Ī┐66╠¢Ż®ųž³cų¦│ųĄ─ųŲ╦ÄŲ¾śIų«ę╗ĪŻ╩Ū║■▒▒╩ĪŲ¾śI╔Ž╩ą▐kųž³cų¦│ųĄ─╔Ž╩ą║¾éõŲ¾śIĪŻ

łD1 ╬õØhÉ█├±ųŲ╦ÄėąŽ▐╣½╦Š
Č■ĪóŲ¾śIą┼Žó╗»æ¬ė├┐é¾w¼FĀŅ
╬õØhÉ█├±ųŲ╦ÄėąŽ▐╣½╦Šūį2006─ĻÅ─▓┐ĻĀŲ¾śI▐DųŲ×ķėąŽ▐ž¤╚╬╣½╦ŠęįüĒŻ¼Ļæ└mķ_╩╝┴╦╣▄└Ēūā▄ē║═ą┼Žó╗»Į©įOŻ¼▓óÅ─2007─Ļķ_╩╝Ż¼ę└šš╣½╦Š╣▄└ĒĄ─ąĶŪ¾Ż¼ų▓Į╔ŽŠĆĖ„ĒŚą┼Žó╗»╣▄└ĒŽĄĮyĄ╚ĪŻ
ļSų°Ų¾śIĄ─░lš╣║═ßt╦ÄąąśIĄ─ĖéĀÄ╝ėäĪŻ¼┐═ė^╔Žī”Ų¾śIĄ─ą┼Žó╗»│╠Č╚ę¬Ū¾įĮüĒįĮĖ▀Ż¼Č°╬õØhÉ█├±ę▓ūźūĪ▀@éĆŲ§ÖCŻ¼ž×Åž³hĄ─╩«┴∙┤¾╠ß│÷Ą─“łį│ųęįą┼Žó╗»Ä¦äė╣żśI╗»Ż¼ęį╣żśI╗»┤┘▀Mą┼Žó╗»Ż¼ū▀ą┬ą═╣żśI╗»Ą└┬Ę”Ą─æ┬įĘĮßśŻ¼ĮY║ŽŲ¾śIĄ─īŹļHŪķørŻ¼Å─╣▄└ĒęÄĘČ╗»║═Š½╝Ü╗»╚ļ╩ųŻ¼▓╔╚Ī“ęį³cĦ├µŻ¼š¹¾w═Ų▀M”Ą─ĘĮĘ©Ż¼Å─╬’┴„╣®æ¬µ£║═ĀIõN╣▄└Ē▓┐Ęųķ_╩╝Ż¼▒³ų°“Įyę╗ęÄäØĪóĘų▓ĮīŹ╩®ĪóŲĮ┼_╝»öĄō■╝»ųą”Ą─ĘĮßśŻ¼Į©įO║══Ļ╔Ų║Ł╔w░³║¼žöäš╣▄└ĒŽĄĮyŻ©ĮĄ¹K3Ż®Īó╬’┴„╣®æ¬µ£╣▄└ĒŽĄĮyĪó│╔▒Š║╦╦Ń╣▄└ĒŽĄĮyĪó╔·«ał╠ąą╣▄└ĒŽĄĮyĪó┘|┴┐Öz£y┼cį┌ŠĆ▒O£yŽĄĮyĪó╦ÄŲĘõN╩█┴„Ž“╣▄└ĒŽĄĮyĪóŠC║ŽĀIõN╣▄└ĒŲĮ┼_Īóčą░l▌oų·╣▄└ĒŲĮ┼_Īó╚╦┴”┘Yį┤┼c┐āą¦┐╝║╦ŽĄĮyĄ╚Ė„ĒŚūėŽĄĮyį┌ā╚Ą─Ų¾śIŠC║Ž╣▄└ĒŲĮ┼_Ż¼īŹ¼Fī”Ų¾śIĄ─▓╔┘ÅĪó╔·«aĪóā”▀\ĪóõN╩█Ą╚╚½▓┐▀^│╠Ą─╚½├µ▒OČĮ┼c╣▄└ĒŻ¼╠ß╔²žöäš│╔▒Š┐žųŲ─▄┴”┼c┘YĮ┐žųŲ─▄┴”Ż¼╝░Ģr▒▄├ŌĖ„ĘNžöäš’LļU║═śIäš’LļUŻ¼▒ŻūCŲ¾śIĄ─┴╝║├▀\ū„ĪŻ
╬õØhÉ█├±ųŲ╦ÄėąŽ▐╣½╦ŠęčĮøĮ©įO┴╦Ė▓╔w╚½ÅSĄ─ėąŠĆŠWĮjŻ¼▓óīŹ¼F┴╦▐k╣½ģ^ė“Ą─¤oŠĆŠWĮjĖ▓╔wŻ¼─┐Ū░š²ęÄäØĮ©įO▀BĮė╚½╣½╦ŠÄ¦PLCĮė┐┌Ą─Ė„ĒŚįOéõĄ─╣żśI┐žųŲŠWĮjĪŻ
╬õØhÉ█├±ųŲ╦ÄėąŽ▐╣½╦Š─┐Ū░ėą3┼_īŻė├Ę■äšŲ„ė├ė┌ų¦ō╬ŽÓæ¬æ¬ė├ŽĄĮyŻ¼Ųõ╦¹ĘŪīŻė├Ę■äšŲ„ė├ļŖ─X4┼_Ż¼╚½╣½╦Šėą145┼_Ė„ĘNą═╠¢Ą─ļŖ─XŻ©║¼╣Pėø▒ŠĪó┼_╩ĮÖCĪó╣żū„šŠŻ¼ę╗░Ń×ķ┬ōŽļĪó╗▌ŲšĄ╚ŲĘ┼ŲÖCŻ®Ż¼╣½╦Šėą2ŚlļŖą┼īŻė├╣Ō└wŻ©ę╗Śl16MŻ¼ę╗Śl4MŻ®ė├ė┌▀BĮėĄĮInternetĪŻ
─┐Ū░Ż¼╬õØhÉ█├±ųŲ╦ÄėąŽ▐╣½╦Šęčėąæ¬ė├ŽĄĮyėąŻ║ĮĄ¹K3žöäš╣▄└ĒŽĄĮyĪóŻŽŻ┴ģf═¼▐k╣½ŽĄĮyĪó╣½╦ŠŠC║Ž╣▄└ĒŲĮ┼_Ą─╬’┴„╣®æ¬µ£╣▄└Ē▓┐ĘųĄ╚Ż¼Ž┬ę╗▓ĮöMöUš╣╣½╦ŠŠC║Ž╣▄└ĒŲĮ┼_Ż¼Ļæ└m╔ŽŠĆ┴„Ž“╣▄└ĒŽĄĮyĪóŠC║ŽĀIõN╣▄└ĒŽĄĮyĪó╔·«ał╠ąą╣▄└ĒŽĄĮyĪó┘|┴┐Öz£y┼cį┌ŠĆ▒O£yŽĄĮyĄ╚Ż¼▀Mę╗▓Į╔²╚AŲ¾śIĄ─ą┼Žó╗»æ¬ė├Ż¼×ķ║¾└mĄ─Ų¾śI╚½├µŅA╦Ń╣▄└Ē┼c╚½åT┐āą¦┐╝║╦╣▄└Ē┤“║├╗∙ĄAĪŻ
╚²Īóģóįuą┼Žó╗»ĒŚ─┐įö╝ÜŪķørĮķĮB
1. ĒŚ─┐▒│Š░ĮķĮB
╦ÄŲĘ┘|┴┐ų┴ĻPųžę¬Ż¼▓╗āHų▒ĮėĻP║§╣½▒ŖĮĪ┐ĄĪó╔·├³░▓╚½Ż¼Ė³ĻP║§╔ńĢ■║═ųC░▓Č©Ż¼ė░Ēæš■Ė«ą╬Ž¾┼cł╠š■─▄┴”Ż¼╚šęµ│╔×ķ╔ńĢ■▌øšō┼c░┘ąšĻPūóĄ─Į╣³cĪŻ³hųąčļĪóć°äšį║ī”╦ÄŲĘ▒O╣▄╣żū„Ė▀Č╚ųžęĢŻ¼ČÓ┤╬ÅŖš{ę¬Å─╔·«aį┤Ņ^┤_▒Ż╦ÄŲĘ░▓╚½ėąą¦Ż¼┘|┴┐┐╔┐žĪŻ
╬ęć°╦ÄŲĘ╔·«aŲ¾śIöĄ┴┐ČÓŻ¼Ęų▓╝ÅVŻ¼░lš╣▓╗Š∙║ŌŻ¼Ūę╦ÄŲĘŲĘĘNČÓĪó䮹═ČÓŻ¼╔·«a╣ż╦ćŽÓī”Å═ļsŻ¼īŻśIąįÅŖŻ¼¼Fėą╦ÄŲĘ╔·«a▒OČĮĘĮ╩Įęį¼Fł÷Öz▓ķ×ķų„Ż¼ė╔ė┌▒O╣▄╚╦åT╔┘Īó╚╬äšųžŻ¼ī¦ų┬▒O╣▄Ņl┬╩Ą═Īó├żģ^ČÓĪŻßt╦Ä╩┬╣╩Įė▀B│÷¼FŻ¼╚ńŻ║08─Ļ4į┬Ż¼²R²R╣■Ā¢Ą┌Č■ųŲ╦ÄÅS╔·«aĄ─“┴┴Š·╝ū╦žūó╔õę║”╩╣öĄ╚╦╦└═÷Ż╗5į┬Ż¼ĮŁ╬„▓®č┼╔·╬’ųŲ╦ÄėąŽ▐╣½╦Š╔·«aĄ─Ą─ņo├}ūó╔õ╚╦├Ōę▀Ū“Ą░░ūūó╔õę║ų┬6╚╦╦└═÷Ż╗10į┬Ż¼║┌²łĮŁ═Ļ▀_╔Į╦ÄśI╣½╦Š╔·«aĄ─┤╠╬Õ╝ė╩▄╬█╚ŠŻ¼ī¦ų┬öĄ░┘╚╦│÷¼F▓╗┴╝Ę┤æ¬Ż¼įŲ─Ž7╚╦╦└═÷Ż¼═Ļ▀_╔Į╣½╦Š▒╗└š┴Ņ╩«─Ļā╚▓╗Ą├Å─╩┬╦ÄŲĘ╔·«aĪóĮøĀI╗ŅäėĪŻå¢Ņ}╦ÄĮė▀B│÷¼FŻ¼ŽŲŲ┴╦╔ńĢ■ī”ßt╦Ä«aŲĘ┘|┴┐Ą─┘|ę╔’L▓©Ż¼ę²░l┴╦ī”╦ÄśI┘|┴┐Ą─ą┼╚╬╬ŻÖCĪŻļSų°▒O╣▄╝░Ų¾śI░lš╣Ą─ąĶ꬯¼ĘŪ¼Fł÷▒O╣▄▒OČĮųŲČ╚æ¬▀\Č°╔·ĪŻ
─┐Ū░Ż¼ć°ā╚ęčėąę╗ą®Ė▀’LļUŅÉ╦ÄŲĘ╔·«aŲ¾śIķ_╩╝įć³c═ŲąąĘŪ¼Fł÷ęĢŅl▒O┐žŽĄĮyŻ¼Ų¾śIį┌ŽÓĻP╔·«a┐žųŲ³c╔Ž░▓čbözŽ±Ņ^Ż¼īó╔·«a¼Fł÷Ą─łDŽ±ą┼Žóé„╦═ĄĮ▒O╣▄╚╦åT▐k╣½╩ę▓óõøŽ±┤µÖnŻ¼╣▄└Ē╚╦åT┐╔═©▀^ęĢŅlĪóõøŽ±▒O╣▄ĪóÖz▓ķ╔·«a▀^│╠ųąĄ─Ė„ĘN▀`ęÄ▓┘ū„Ż¼ÅŖ╗»▒O╣▄▓┐ķTĄ─▒O╣▄┴”Č╚╝░╣żū„Ą─╝░ĢrąįŻ¼Ę└ų╣å¢Ņ}╦ÄŲĘ«aŲĘ┴„Ž“╩ął÷ĪŻĘŪ¼Fł÷ęĢŅl▒O┐žį┌ę╗Č©│╠Č╚ĮŌøQ┴╦─┐Ū░▒O╣▄ÖCśŗ▒O╣▄╚╦┴”╬’┴”▓╗ūŃĄ─å¢Ņ}Ż¼īŹ¼F┴╦╦ÄŲĘ╔·«a┘|┴┐Ą─╩┬ųąŅAŠ»║═╩┬║¾å¢Ņ}ūĘ╦▌Ą─▒O╣▄┬Ü─▄ę¬Ū¾Ż╗Ą½╬┤─▄Å─Ė∙į┤╔ŽĮŌøQ╦ÄŲĘ╔·«a▒O╣▄Ą─ŽĄĮyąįå¢Ņ}Ż¼▒O┐ž╚╦åTĄ─╣żū„┴┐▓╗Ą½ø]ėą£p╔┘Ż¼╣żū„ÅŖČ╚Ę┤Č°╝ė┤¾Ż¼ž¤╚╬ą─ę¬Ū¾Ė³Ė▀Ż¼╩┬║¾Ęų╬÷▓ķ┐┤ęĢŅlõøŽ±┘MĢr┘M┴”ĪŻČ°Ūęī”Ų¾śIüĒšfŻ¼«ö░l¼Få¢Ņ}ĢrŻ¼╔·«aęč═Ļ│╔Ż¼ōp╩¦ęč▓╗┐╔▒▄├ŌĪŻ
ļSų°ßt╦ÄąąśIĮøØ·Ą─┐ņ╦┘░lš╣Ż¼Ų¾śI╣▄└Ē└Ē─Ņę▓į┌▓╗öÓ░lš╣ūā╗»ųąŻ¼ĘŪ¼Fł÷▒O╣▄ęč│╔×ķę╗ĘN▒ž╚╗Ą─░lš╣┌ģä▌Ż¼─┐Ū░ć°ā╚ę╗ą®Ų¾śI▓╔ė├Ą─ĘŪ¼Fł÷ęĢŅl▒O┐žŽĄĮy▀Ć▓╗─▄Å─Ė∙į┤╔ŽØMūŃŲ¾śI╣▄└ĒĄ─ąĶŪ¾ĪŻČ°ć°═Ō▓╔ė├Ą─īŹĢröĄō■▒O┐žŽĄĮyŻ¼ļm╚╗īŹ¼F┴╦╩┬╣╩╩┬Ū░ŅAŠ»Ż¼Ą½▒O┐žŽĄĮyų▒Įė║═įOéõĮM│╔ę╗¾wŻ¼Ūę├┐Śl╔·«aŠĆĄ─öĄō■▒O┐žČ╝╩Ū¬Ü┴ó▀\ąąĄ─Ż¼╔·«a│╔▒ŠĘŪ│ŻĖ▀ĪŻ
2. ĒŚ─┐─┐ś╦┼cīŹ╩®įŁät
ĒŚ─┐─┐ś╦
1)ÜW├╦GMPī”Ų½▓Ņ╠Ä└ĒęÄČ©Ż¼╦∙ėąŲ½▓ŅČ╝æ¬įōš{▓ķŪÕ│■▓ó▓╔╚ĪŽÓĻPĄ─╝mŲ½┤ļ╩®Ż¼▓óį┌┤_šJī”«aŲĘĄ─┘|┴┐ø]ėąė░Ēæ║¾Ż¼ĘĮ┐╔Ę┼ąą│╔ŲĘĪŻŽĄĮy═©▀^¼Fł÷ą┼ŽóĄ─īŹĢr▓╔╝»Ż¼ī”ė┌┘|┴┐å¢Ņ}Ą─┤_Č©ĪóįŁę“Īó▓©╝░Ą─ĘČć·īŹ¼F┐ņ╦┘£╩┤_Č©╬╗▓óīŹ¼F«aŲĘļ[╗╝Ą─ūĘ╦▌║═Ęų╬÷Ż¼ī”╣ż╦ć▀^│╠Ą─ĘĆČ©ąįŻ¼«aŲĘ┴╝┬╩Īó▓╗┴╝╚▒Ž▌Ęų▓╝Ą─▓©äėĀŅør▀MąąīŹĢr▒O┐žĪŻ
2)▀\ė├ėŗ╦ŃÖCŠWĮj╝╝ągŻ¼īó▒O┐žöĄō■┤µā”▀MŽĄĮyŻ¼▒O╣▄╚╦åT┐╔ļSĢrļSĄžšŲ╬š╔·«aĄ─ūŅą┬öĄō■Ż¼īŹ¼Fī”Ų¾śI╔·«a╚½▀^│╠Ą─▀h│╠īŹĢr▒O┐žŻ¼┤¾┤¾╠ßĖ▀╦ÄŲĘ┘|┴┐┐žųŲĄ─Ģrą¦ąįĪŻ
3)└¹ė├ųŪ─▄╗»Ą─╝»│╔╝╝ągŻ¼īŹ¼F╔·«a«É│ŻĀŅæBĪóļ[╗╝╩┬Ū░ŅAŠ»Ż¼Č┼Į^▓╗║ŽĖ±«aŲĘĄ─│÷¼FŻ¼īŹ¼F╔·«a“┴Ń╚▒Ž▌”Ż╗
4)ÜW├╦GMPšJ×ķ╝ā╗»╦«Ą─PHųĄĪóļŖī¦┬╩╝░┘A┤µ£žČ╚╚²éĆųĖś╦Ż¼▒žĒÜįOėąį┌ŠĆ▒O┐ž┤ļ╩®Ż¼į┘│÷¼Få¢Ņ}Ģrł¾Š»ĪŻŽĄĮyīŹ¼Fųž³cįOéõŻ©Ž┤Ų┐ÖCŻ¼╦ĒĄ└║µŽõŻ¼╣ÓčbÖCŻ¼ā÷Ė╔ÖCĪó▄ł╔wÖCŻ¼─z╚¹ŪÕŽ┤ÖCŻ¼õX╔wŪÕŽ┤ÖCŲ„Ż¼Ė╔¤ß£ńŠ·╣±Īóر¤ß£ńŠ·╣±Īó┼õ┴ŽŽĄĮyĄ╚Ż®öĄō■▓╔╝»╝░ł¾▒Ē▌ö│÷Ż╗
5)ŽĄĮy╔·«aöĄō■ĮYśŗ╗»Ż¼╝╚┐╔ęįė├ė┌Ų¾śIĄ─Ė„ĘNöĄō■═┌Š“Ęų╬÷Ż¼ā×╗»Ų¾śI╔·«a┴„│╠Ż╗ėųĘŪ│ŻĘĮ▒Ń┘|┴┐▒O╣▄▓┐ķT▀Mąą┘|┴┐įu╣└║═å¢Ņ}╦▌į┤Ż╗
6)×ķŅIī¦╠ß╣®øQ▓▀ą┼Žóų¦│ųŻ¼īóŅIī¦øQ▓▀╦∙ąĶĄ─Ė„ĘNą┼ŽóĮø▀^ģR┐é╠Ä└ĒŻ¼ęįĖ„ĘNų▒ė^Ą─ĘĮ╩Į’@╩ŠŻ¼╠ßĖ▀ŠC║ŽĘų╬÷║═øQ▓▀ų¦│ų─▄┴”Ż╗
7)ęį╔·«a▀\ąą▒O┐ž×ķ║╦ą─Ż¼ęį╔·«a┼·┤╬×ķå╬╬╗Ż¼ėøõø┼·┤╬╔·«a▀^│╠ųąĖ„éĆėŗ┴┐╣żŠ▀Ą─īŹĢröĄō■Ż¼Å─Č°š╣¼F«öĢr╔·«aŁhŠ│Ą─£žČ╚┼cرČ╚öĄō■Ż¼ģfų·╣▄└Ē╚╦åT▀MąąöĄō■Ęų╬÷Ż¼ŽĄĮy╩╝ĮKž×Åžė├öĄō■šfįÆŻ¼ęįöĄō■×ķś╦£╩Ą─įŁätŻ¼ūó╚ļĖ„ĘNöĄō■ÖÓŽ▐Ż¼ęį▒ŻūCöĄō■ėąą¦ąįĪŻ
īŹ╩®įŁät
ĮY║Ž╔·«a▒O┐žĘĮ╩Į╝░╬ęć°¾wųŲĪóėŗ╦ŃÖC▄ø╝■╝╝ągĄ─░lš╣Ż¼▒Šų°┘Yį┤│õĘų└¹ė├Ą─įŁätŻ¼ĘŪ¼Fł÷īŹĢr╣▄└ĒūŅĮKæ¬īŹ¼F“╣▄”“┐ž”ę╗¾w╗»Ż¼Š▀¾w░³║¼ęįŽ┬ÄūéĆĘĮ├µŻ║
ĘŪ¼Fł÷īŹĢr╣▄┐žŽĄĮyĄ─Web╗»
┐ńŲĮ┼_Ą─Web╝▄śŗ╝╝ągĄ─│╔╩ņ░lš╣×ķĘŪ¼Fł÷īŹĢr╣▄┐žŽĄĮyĄ─Web╗»╠ß╣®┴╦╝╝ągŚl╝■ĪŻ═¼ĢrŻ¼ĘŪ¼Fł÷īŹĢr╣▄┐žŽĄĮyę▓š²į┌Ž“═Ō░³╗»ĘĮŽ“░lš╣Ż¼┐ńć°╝»łF╣½╦Š└¹ė├ÅVė“ŠW╝╝ągīŹ¼Fī”╔·«a▀^│╠Ą─╩▄┐ž╣▄└ĒŻ¼╠ß│÷┴╦ī”ĘŪ¼Fł÷īŹĢr╣▄┐žŽĄĮyWeb╗»Ą─ąĶŪ¾ĪŻę“┤╦Ż¼ĘŪ¼Fł÷īŹĢr╣▄┐žŽĄĮyĄ─Web╗»╩Ūę╗éĆ▒ž╚╗Ą─░lš╣┌ģä▌ĪŻį┌╗∙ė┌WebĄ─ĘŪ¼Fł÷īŹĢr╣▄┐žŽĄĮyų¦│ųŽ┬Ż¼Ų¾śI┐╔ęį═©▀^ŠWĮjī”╔·«a▀^│╠▀Mąą╩▄┐ž╣▄└ĒŻ¼īŹĢr½@╚Ī╦∙ĻPūóĄ─öĄō■Īół¾▒ĒĄ╚ą┼ŽóŻ¼ę▓┐╔ęįī”╔·«a▀^│╠▀MąąĘŪ¼Fł÷Ą─īŹĢr╣▄┐žĪŻ
╔·«a▀^│╠Ą─īŹĢr╣▄┐ž
ĘŪ¼Fł÷īŹĢr╣▄┐žŽĄĮyųąĄ─║╦ą──ŻēKų«ę╗╩ŪīŹĢr▒O┐žŻ¼└¹ė├ųŪ─▄╗»Ą─╝»│╔╝╝ągŻ¼īŹ¼Fčbų├╔·«a╝»ųą┐žųŲĪóŲ¾śI╔·«aäėæB╣▄└ĒŻ╗ėąą¦Ą─ȶųŲė╔ė┌▓┘ū„▓╗«ö║═╚╦×ķĄ─×^┬Ü╗“ŽĄĮyįOéõ▒Š╔ĒČ°įņ│╔╩┬╣╩Ą─░l╔·Ż╗▒O£y╣ż╦ć▀^│╠║═įOéõĀŅæBŻ¼ūŅ┤¾Ž▐Č╚Ąž▒▄├Ō╩┬╣╩Ą─░l╔·ĪŻ
īóŲĘ┘|╣▄└Ē┼c╔·«a▀\ąą╣▄└ĒĄ─└Ē─Ņ╚┌╚ļĄĮīŹļH╣żū„ųąŻ¼╝ė╦┘Ų¾śIŲĘ┘|╣▄└ĒĄ─īŹ╩®╦┘Č╚Ż¼Ä═ų·╣▄└ĒīėĖ³║├Ą─šŲ╬š╣żÅS╔·«aöĄō■ųĖī¦╔·«aĪŻ
ūŅ┤¾│╠Č╚Ą─æ¬ė├╝»│╔╗»
─┐Ū░Ą─ĘŪ¼Fł÷īŹĢr▒O┐žŽĄĮy╚į╚╗┤µį┌ą┼Žó╣┬Źuå¢Ņ}ĪŻŲ¾śIą┼Žó╗»ŽĄĮyš²į┌ū▀Ž“öĄō■ą┼Žó┼c╣▄└ĒśI䚥─š¹║Ž┼c╝»│╔Ż¼╩╣ą┼ŽóĄ├ĄĮĖ▀Č╚╣▓ŽĒŻ¼ęį▒ŃĮŌøQČÓéĆ«ÉśŗŽĄĮyĄ─ą┼Žó┘Yį┤Ą─Ė▀ą¦└¹ė├å¢Ņ}ĪŻę“┤╦Ż¼ĘŪ¼Fł÷īŹĢr╣▄┐žŽĄĮyę▓▒žĒÜ│»æ¬ė├╝»│╔╗»ĘĮŽ“░lš╣Ż¼╩╣Ųõ┼cŲ¾śIĄ─ERPŽĄĮyĪóMESŽĄĮyĪóĖ„éĆå╬ĒŚĄ─ūėŽĄĮy(╚ńžö䚎ĄĮyĪó╬’┘YŽĄĮyĪó╔·«aŽĄĮyĪó╚╦┴”┘Yį┤ŽĄĮyĄ╚)ęį╝░¼Fł÷▒O£yŽĄĮy(╚ńDCS,PLCĪóĀŅæB▒O£yŽĄĮyĄ╚)ų«ķgīŹ¼FūŅ┤¾│╠Č╚Ą─æ¬ė├╝»│╔ĪŻ
3. ĒŚ─┐īŹ╩®┼cæ¬ė├Ūķørįö╝ÜĮķĮB
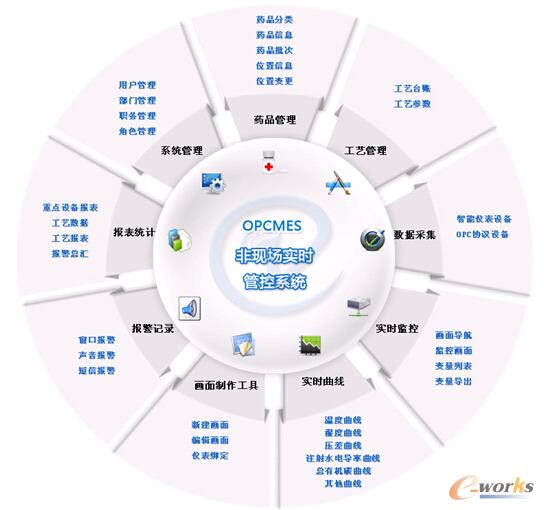
łD2 ╣”─▄─ŻēK
╣”─▄Ė┼╩÷Ż║▒ŠŽĄĮyęįųž³cįOéõ╝░╣ż╦ćģóöĄĄ─öĄō■▓╔╝»ĪóīŹĢr▒O┐žĪóöĄō■Ęų╬÷×ķ║╦ą─śI䚯¼Ųõ║╦ą─śI䚥─ŽĄĮyĮYśŗłD╚ńłD3ĪŻ
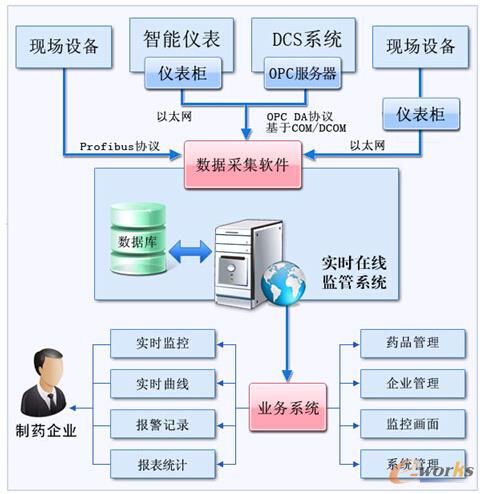
łD3 ║╦ą─śI䚥─ŽĄĮyĮYśŗ
╦ÄŲĘ╣▄└ĒŻ║╦ÄŲĘ╣▄└Ē─ŻēKĮ©┴óųŲ╦ÄŲ¾śIĄ─╦ÄŲĘ╗∙ĄAöĄō■ÄņŻ¼░³└©įö╝ÜĄ─╦ÄŲĘĘųŅÉŻ¼│Żė├Ą─╦ÄŲĘą┼ŽóŻ¼ęį╝░Įø│Żūā╗»Ą─╦ÄŲĘ┼·╠¢ĪŻ
╦ÄŲĘĘųŅÉŻ║╦ÄŲĘĘųŅÉĮ©┴ó║═Č©┴xŲ¾śI╔·«aĄ─╦ÄŲĘĘųŅÉśõŻ¼▒Ńė┌ī¦║Į║═×gė[ĪŻ
╦ÄŲĘą┼ŽóŻ║╦ÄŲĘą┼ŽóįOų├Ų¾śI╔·«aĄ─╦ÄŲĘą┼ŽóŻ¼░³└©╦ÄŲĘ├¹ĘQĪóęÄĖ±ą═╠¢Ą╚ą┼ŽóĪŻ
╦ÄŲĘ┼·┤╬Ż║╦ÄŲĘ┼·┤╬▀Ć░³└©┼·┤╬Īó┼·┴┐Īó╔·«a╚šŲ┌Ą╚ą┼ŽóĪŻ├┐éĆ╦ÄŲĘ┼·┤╬┤µā”į┌Ę¹║ŽęÄČ©ŁhŠ│ģóöĄĄ─é}Äņā╚Ż¼ŽĄĮy═©▀^īŹĢr▒O┐ž½@╚Ī╣ż╦ćģóöĄöĄō■Ż¼▒ŻūC╦ÄŲĘ┼·┤╬Ę¹║Ž┤µā”ŁhŠ│ę¬Ū¾ĪŻ╦ÄŲĘ┼·┤╬ąĶę¬┤_Č©į┌ųŲ䮊Ć╗“š▀é}ÄņĄ─ķ_╩╝║═ĮY╩°ĢrķgŻ¼ęį╝░╩Ūʱį┌╬╗Ą─ĀŅæBŻ¼ė├æ¶═©▀^īŹļHŪķør╠Ä└Ē╦ÄŲĘ┼·┤╬Ą─╬╗ų├ūāĖ³╣▄└ĒĪŻ
╬╗ų├ą┼ŽóŻ║╬╗ų├ą┼Žó─ŻēKČ©┴x╦ÄŲĘ╔·«aŠĆĪó┤µā”é}ÄņĄ─╬╗ų├ą┼ŽóŻ¼Å─Č°▒ŻūCāx▒ĒģóöĄ║═▓╔╝»öĄō■Ą─ĻP┬ōĪŻ
╬╗ų├ūāĖ³Ż║╬╗ų├ūāĖ³ėøõø├┐ę╗╦ÄŲĘ┼·┤╬Å─╔·«aŠĆĄĮé}ÄņĄ─╬╗ų├ūā╗»Ż¼ęį╝░į┌▄ćķgĄ─┴„Ž“ĪŻ
╣ż╦ć┼_ÄżŻ║╣ż╦ć┼_Äżų„ę¬╩Ūīó╔·«aŲ¾śIŽÓĻPĄ─╣ż╦ć╬─Ön▀MąąÖn░Ė╣▄└ĒŻ¼░³└©╝╝ągęÄ│╠Īó▓┘ū„Ę©Īó╣ż╦ć┐©Ų¼Īó╝╝ąg┼_ÄżĪóÖz▓ķ┐╝║╦Īó╝╝ągĘĮ░ĖĪóś╦£╩│╠ą“┐©╝░Öz▓ķĶbČ©Ą╚Ż¼īŹ¼F╣ż╦ćą┼Žó┘Yį┤╣▓ŽĒŻ¼▓óŪę┐╔ęį═©▀^łD╝łĻP┬ōĄĮī”æ¬Ą─╣ż╦ćą┼Žó╝░ĻP┬ōłD╝łųąłD╦žī”æ¬Ą─įOéõ╣ż╦ćą┼ŽóĪŻ
╣ż╦ćģóöĄŻ║╣ż╦ćģóöĄČ©┴x▓╔╝»ĒŚĄ─╗∙▒Šą┼ŽóŻ¼░³└©╦∙ī┘āx▒ĒĄ─Å─ÖCĄžųĘŻ¼³S╔½Īó╝t╔½Š»ĮõŠĆĄ─ģ^ķgĘČć·Ż¼╦∙ī┘Ą─é}ÄņĄ╚ĪŻ╣ż╦ćģóöĄĄ─╝t³SŠ»ĮõŠĆė├ė┌ł¾Š»║═ųĖś╦▒╚ī”Ęų╬÷ĪŻę╗░ŃŻ¼╣ż╦ćģóöĄĄ─ą┼ŽóČ©┴x║¾▓╗ę¬▀Mąąą▐Ė─ĪŻ
öĄō■▓╔╝»Ż║öĄō■▓╔╝»▄ø╝■ė├ė┌▓╔╝»ūįäė╗»╔·«aŽĄĮyĄ─īŹĢr╣ż╦ćöĄō■ĄĮŲ¾śIśI䚎ĄĮyųąŻ¼▓óŪę▀Mąąėŗ╦ŃĪóĘų╬÷Īó╠Ä└ĒŻ¼ū„×ķŲ¾śI╣▄└Ē╚╦åTĄ─øQ▓▀ģó┐╝ę└ō■ĪŻįō▄ø╝■ū„×ķOPCMESŽĄĮyĄ─ĄūīėöĄō■╠Ä└Ē║╦ą──ŻēKŻ¼╚½├µ╠Ä└ĒŽĄĮy┼cįOéõĄ─öĄō■Įė┐┌Ż║ę╗ĘĮ├µų¦│ų░³║¼ModbusģfūhĪóOPCģfūhęį╝░ProfibusģfūhĄ╚ś╦£╩ģfūhĄ─Ė„ĘNāx▒ĒįOéõŻ╗┴Ēę╗ĘĮ├µŻ¼ī”ė┌ĘŪś╦£╩ģfūhĄ─įOéõ╗“š▀ĘŪ│ŻęÄöĄō■Ż©▒╚╚ńę║╬╗Īó▐D╦┘Ż®Ą─▓╔╝»Ż¼įō▄ø╝■─ŻēK╠ß╣®╚½├µĄ─ė▓╝■ĮŌøQĘĮ░Ė——Č©ųŲPLC┐╔ŠÄ│╠┐žųŲ╣±īŹ¼F┼cįOéõĄ─┐žųŲīėĄ─═©ą┼═Ļ│╔öĄō■Ą─▓╔╝»ĪŻ┐╔▓╔╝»Ą─öĄō■ģóöĄ░³║¼ŁhŠ│£žØ±Č╚Īóē║▓ŅĪó’L╦┘Ż¼╔·«aė├╦«ļŖī¦┬╩ĪóTOC╝░Ųõ╦¹╠žĘNįOéõĄ─GMP┐žųŲģóöĄĪŻ
öĄō■▓╔╝»ĘĮ░ĖŻ║╣żśI┐žųŲś╦£╩═©ą┼ģfūhŻ║OPCģfūhĪóModbusģfūhĪóProfibusģfūhŻ╗
ĘŪś╦ģfūhĄ─╠žĘNįOéõŻ║Č©ųŲPLC┐╔ŠÄ│╠┐žųŲ╣±ū„×ķöĄō■▓╔╝»═©ą┼ųąķg╝■Ż╗
ęĢŅl▒O┐žŻ║×ķĖ³║├Ą─Ēææ¬ć°╝ę╦Ä▒OŠųĄ─▓┐╩ę¬Ū¾Ż¼į┌╚š│Ż▒O╣▄ųąūóųž’LļU╣▄└ĒŻ¼äōą┬▒O╣▄─Ż╩ĮŻ¼ĘeśO╠Į╦„ī”Ė▀’LļUŲĘĘN╦ÄŲĘ╔·«aŲ¾śIīŹ╩®¼Fł÷▒O┐ž║═ĘŪ¼Fł÷▒O┐žŽÓĮY║ŽĄ─▒O╣▄─Ż╩ĮŻ¼īóęĢŅl▒O┐ž╝{╚ļš¹éĆśIäšŲĮ┼_ųąŻ¼ė├ė┌īŹ¼Fī”ĻPµIŹÅ╬╗ĪóĻPµIģ^ė“╝░ĻPµI▓┘ū„Ą─24ąĪĢręĢŅlīŹĢr▒O┐žŻ¼▓ó╝░Ģr▒Ż┤µęĢŅl┘Y┴ŽŻ¼┐╔▀MąąęĢŅl▒O┐žįOų├ĪóīŹĢr«ŗ├µŪąōQ×gė[╝░Üv╩ĘęĢŅl┘Y┴ŽÖz╦„Ą╚▒O┐ž▓┘ū„ĪŻęĢŅl▒O┐žÖÓŽ▐┼cŽĄĮyÖÓŽ▐ę╗ų┬ĪŻęĢŅl▒O┐ž╣”─▄ūįäė║═╔·«a╣ż╦ćģóöĄ▒O┐žĮY║ŽŻ¼īŹ¼F╔·«a╣ż╦ćģóöĄł¾Š»Ż¼ęĢŅl▒O┐žūįäėŪąōQų┴įōģ^ė“▒O┐žŻ¼▀_ĄĮęĢŅl║═öĄō■Ą─╚½├µĮY║ŽĪŻ
ī”ė┌ęčĮø┤µį┌▒O┐žŽĄĮyĄ─Ų¾śIė├æ¶Ż¼┐╔╔²╝ē▓┐Ęų▓┐╝■╩╣ų«ų¦│ųŠWĮjģfūhŻ¼īó▒O┐ž«ŗ├µ╝»│╔ė┌OPCMESŽĄĮyŻ╗ī”ė┌╬┤░▓čbęĢŅl▒O┐žĄ─Ų¾śIė├æ¶Ż¼OPCMESŽĄĮyīó╠ß╣®╚½ą┬Ą─ęĢŅlĮŌøQĘĮ░ĖĪŻ
īŹĢr▒O┐žŻ║īŹĢr▒O┐ž╩ŪśI䚎ĄĮyĮKČ╦ė├æ¶╩╣ė├Ą─║╦ą─▄ø╝■Ż¼┐╔ęįīŹĢr×gė[ųž³cįOéõŻ©ā÷Ė╔ÖCĪóĖ╔¤ß£ńŠ·╣±Īóر¤ß£ńŠ·╣±Īó╣ÓčbÖCĄ╚Ż®Īóāx▒ĒŻ©£žØ±Č╚Īóē║▓ŅĪó’L╦┘Ą╚Ż®Īóūó╔õ╦«Ą─ļŖī¦┬╩╝░┐éėąÖC╠╝öĄō■Ż¼▀Mąą«ŗ├µī¦║ĮŻ¼ęį╝░▓ķ┐┤ūā┴┐┴ą▒ĒĪóīŹĢrŪ·ŠĆĪół¾Š»ėøõøĄ╚ŽÓĻPą┼ŽóĪŻ▒O┐ž«ŗ├µ║═╣żÅSĄ─įOéõ╬╗ų├Īó╣ż╦ć┴„│╠ę╗ų┬Ż¼┐╔ęįą╬Ž¾Īóų▒ė^Ą─Ę┤欫öŪ░įOéõĪóūó╔õ╦«Ą─ļŖī¦┬╩╝░┐éėąÖC╠╝Ą─ĀŅæBĪŻ▒O┐ž«ŗ├µ╗∙ė┌Web╝╝ągŻ¼ė├æ¶┐╔ęįį┌ĘŪ¼Fł÷ŪķørŽ┬▀Mąą┐ņ╦┘▒OęĢįOéõĀŅæBŻ¼╠ßĖ▀╔·«aą¦┬╩ĪŻ
īŹĢrŪ·ŠĆŻ║īŹĢrŪ·ŠĆłDĖ∙ō■╣ż╦ćģóöĄĄ─▓╔╝»ų▄Ų┌Ż¼ų▄Ų┌ąį’@╩Š╣ż╦ćöĄō■Ż¼Å─Č°ą╬│╔īŹĢrŪ·ŠĆĪŻį┌īŹĢrŪ·ŠĆųąŻ¼ė├æ¶┐╔ęį┐┤│÷╣ż╦ćģóöĄĄ─┌ģä▌ĀŅæBŻ¼╩Ūī┘ė┌ŲĮĘĆą═ĪóŽ┬ĮĄą═╗“š▀╔Ž╔²ą═Ż¼Å─Č°╠ßŪ░▓╔╚Īėąą¦┤ļ╩®▒ŻūC╣ż╦ćģóöĄĄ─ŲĮ║ŌĘĆČ©Ż╗ė├æ¶┐╔ęį┐┤│÷ūŅĮ³ĢrķgČ╬Ą─öĄō■║═ł¾Š»╔ŽŽ┬ųĄĄ─ī”▒╚ĻPŽĄĪŻ
ł¾Š»ėøõøŻ║ł¾Š»ėøõø─ŻēKūįäėėøõø╣ż╦ćģóöĄ│¼▀^Š»ĮõŠĆįō╩┬╝■Ą─įö╝Üą┼ŽóŻ¼░³└©╩┬╝■░l╔·Ą─ķ_╩╝ĢrķgŻ¼ęį╝░╩┬╝■Ą─┤_šJ╚╦Īó┤_šJĢrķgŻ¼▀Ćėą╣ż╦ć╗ųÅ═ĄĮš²│ŻųĄĄ─ĮY╩°ĢrķgĪŻÅ─Č°Ż¼ŽĄĮyįö╝ÜūĘ╦▌ł¾Š»ėøõøĄ─įö╝Üą┼ŽóĪŻ
ŽĄĮy╠ß╣®ČÓĘNĘĮ╩Įī”│¼▀^³S╔½Š»ĮõŠĆĄ─╣ż╦ćöĄō■▀Mąął¾Š»Ż¼Å─Č°▒ŻūCė├æ¶─▄ē“╝░Ģr╠Ä└Ēł¾Š»╩┬╝■Ż¼▀Mę╗▓Įā×╗»ŁhŠ│ģóöĄĘ¹║Žš²│Żę¬Ū¾ĪŻČ╠ą┼ł¾Š»Ż¼┐╔ęįūīāxŲ„āx▒Ēžōž¤╚╦╝░Ģr═©▀^╩ųÖCĘĮ╩Į░l¼F╣ż╦ćģóöĄ│¼│÷š²│ŻĘČć·ĪŻī”ė┌ę╣ķgĢrķgĪóų▄─®Ģrķg╗“š▀╣Ø╝┘╚š╬┤╔Ž░ÓĢrķgĄ╚─▄ē“┐ņ╦┘═©ų¬žōž¤╚╦Ż¼▒▄├Ōå¢Ņ}Ą─░l╔·ĪŻČ╠ą┼ł¾Š»Ż¼ąĶę¬▓╔╝»▄ø╝■╝»│╔Č╠ą┼žłįOéõ▀MąąīŹĢr░l╦═Č╠ą┼ĪŻ┬Ģ궳¾Š»Ż¼─▄ē“į┌¼Fł÷═©▀^└«░╚Īó궎õ░l╔·ėąą¦═©ų¬▄ćķgĄ─╣żū„╚╦åTĪŻ┤░┐┌ł¾Š»Ż¼─▄ē“┐ņ╦┘╠ßąčį┌ŠĆė├æ¶Ż¼Å─Č°╝░Ģr▀Mąą╠Ä└ĒĪŻ
╣ż╦ćöĄō■ĮyėŗŻ║╣ż╦ćöĄō■─ŻēK┐╔ęįī”Ė„┼·┤╬Ą─╦ÄŲĘ▀Mąą╣ż╦ćöĄō■Ęų╬÷Ż¼Ė∙ō■īŹļHąĶꬥ─▓ķįāŚl╝■Ż©┼·┤╬ĪóĢrķgČ╬Ż®Ż¼š╣¼FöĄō■┴ą▒ĒĪóÜv╩ĘŪ·ŠĆĪŻ
Üv╩ĘŪ·ŠĆĘų╬÷ų„ę¬╩ŪĖ∙ō■╣ż╦ć╝░įOéõģóöĄĄ─▓╔╝»ų▄Ų┌Ż¼ų▄Ų┌ąį’@╩Š╣ż╦ć╝░įOéõöĄō■Ż¼Å─Č°ą╬│╔īŹĢrŪ·ŠĆĪŻį┌īŹĢrŪ·ŠĆųąŻ¼ė├æ¶┐╔ęį┐┤│÷╣ż╦ć╝░įOéõģóöĄĄ─┌ģä▌ĀŅæBŻ¼╩Ūī┘ė┌ŲĮĘĆą═ĪóŽ┬ĮĄą═╗“š▀╔Ž╔²ą═Ż¼Å─Č°╠ßŪ░▓╔╚Īėąą¦┤ļ╩®▒ŻūC╣ż╦ć╝░įOéõģóöĄĄ─ŲĮ║ŌĘĆČ©Ż╗ė├æ¶┐╔ęį┐┤│÷ūŅĮ³ĢrķgČ╬Ą─öĄō■║═ł¾Š»╔ŽŽ┬ųĄĄ─ī”▒╚ĻPŽĄĪŻ
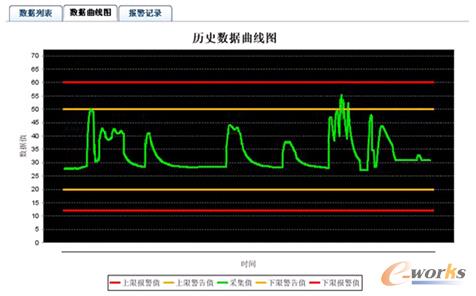
łD4 Üv╩ĘŪ·ŠĆ
╣ż╦ćł¾▒ĒŻ║╣ż╦ćł¾▒Ē─ŻēKė├ė┌×gė[Īó▓ķįāĪóī¦│÷▓╔╝»Ą─öĄō■Ż¼ŽĄĮy╠ß╣®ČÓĘNŚl╝■▀MąąöĄō■▓ķįāŻ¼░³└©╦ÄŲĘĘųŅÉĪó╦ÄŲĘą┼ŽóĪó╦ÄŲĘ┼·╠¢Īó╣ż╦ćģóöĄĪóĢrķgĘČć·Ą╚Śl╝■ĪŻ
╣ż╦ćł¾▒Ē┐╔ęį╔·│╔Ū·ŠĆłDŻ¼▓ó┐╔ęįī¦│÷ExcelĖ±╩ĮĄ─öĄō■ł¾▒ĒĪŻ
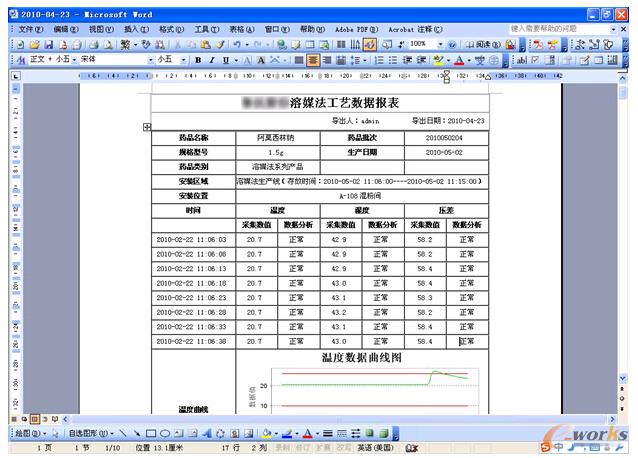
łD5 ╣ż╦ćöĄō■ł¾▒Ē
ųž³cįOéõöĄō■▓╔╝»Ż║┐╔ęįī”ųž³cįOéõŻ¼╚ń┼õ┴ŽŽĄĮyŻ¼╦«ŽĄĮyŻ¼Ž┤Ų┐ÖCŻ¼╣ÓčbÖCŻ¼ā÷Ė╔ÖCŻ¼▄ł╔wÖCŻ¼£ńŠ·╣±Ą╚Ą─ŽÓĻPģóöĄ▀Mąą▓╔╝»Ż╗
ŽĄĮy┐╔ęįĘų×ķŁhŠ│ŽĄĮyŻ©ēm░Ż┴ŻūėŻ¼£žØ±Č╚Ż¼ē║▓ŅŻ¼’L╦┘Ą╚Ż®Ż¼įOéõŽĄĮyŻ©Ž┤Ų┐ÖCŻ¼╣ÓčbÖCŻ¼ā÷Ė╔ÖCŻ¼▄ł╔wÖCŻ¼£ńŠ·╣±Ą╚Ż®Ż¼╣½ė├ŽĄĮyŻ©ūó╔õ╦«Ż¼╝ā╗»╦«ŽĄĮyĄ╚Ż®ĪŻ
ųž³cįOéõł¾▒Ē─ŻēKė├ė┌×gė[Īó▓ķįāĪóī¦│÷ųž³cįOéõ▓╔╝»Ą─öĄō■Ż¼ŽĄĮy╠ß╣®ČÓĘNŚl╝■▀MąąöĄō■▓ķįāŻ¼░³└©▄ćķgĪóįOéõĘųŅÉĪóģóöĄ╝░ĢrķgĘČć·Ą╚Śl╝■ĪŻųž³cįOéõł¾▒Ēł¾▒Ē┐╔ęį╔·│╔Ū·ŠĆłDŻ¼▓ó┐╔ęįī¦│÷ExcelĖ±╩ĮĄ─öĄō■ł¾▒ĒĪŻ
ł¾Š»ģR┐éŻ║ł¾Š»ģR┐é─ŻēKė├ė┌ī”╣ż╦ć╝░įOéõ▓╔╝»«É│ŻöĄō■▀MąąĘų╬÷ĪóģR┐éŻ¼═©▀^Ė„ŅÉ▓ķįāŚl╝■ĪóģóöĄĘųŅÉĪó╬╗ų├ĘųŅÉ▀MąąöĄō■š╣¼FŻ¼▒Ńė┌╔·«a╚╦åT┴╦ĮŌįö╝ÜĄ─╔·«a¼Fł÷öĄō■Ż¼Ė─▀M╣ż╦ć╝░įOéõ┤ļ╩®Ż¼▒ŻūC╦ÄŲĘ╔·«aĄ─┘|┴┐ĪŻ
ŽĄĮy╣▄└ĒŻ║ŽĄĮy╣▄└Ē─ŻēKė├ė┌▀MąąŽĄĮyĄ─╗∙▒Š┼õų├Ż¼ė├æ¶┐╔ęį╩╣ė├įō╣”─▄Į©┴ó╣½╦Š▓┐ķTÖCśŗĪó╚╦╩┬ą┼ŽóĪóĮŪ╔½Ęų╬÷ĪóČ©┴x╗∙ĄAöĄō■Ż©└²╚ńīWÜvĪó┬ÜĘQĪó┬ÜäšĪóš■ų╬├µ├▓Īó├±ūÕĪóėŗ┴┐å╬╬╗Ą╚Ż®Ą╚ĪŻ╩╣ė├ŽĄĮy╣▄└ĒĄ─╣”─▄Ż¼ė├æ¶▀Ć┐╔ęį▀Mąą▒╗ŲŲē─öĄō■Ą─╗ųÅ═Ż¼Č©┴xÖÓŽ▐▒ĒŻ¼Č©┴x╣żū„┴„Ą╚ĪŻ
ĮM┐ŚÖCśŗŻ║Č©┴xęį╣½╦Š×ķĖ∙Ą─Ż¼╣½╦ŠŽ┬Ė„▓┐ķT×ķĘųų¦Ą─ĮM┐ŚÖCśŗśõĪŻīó╣½╦Š¼FėąĄ─Ė„┬Ü─▄▓┐ķTČ©┴xĄĮŽĄĮyųąĪŻ
ÖÓŽ▐┼cĮŪ╔½Ż║═©▀^īó╣”─▄┼cöĄō■ÖÓŽ▐ĮēČ©ĄĮĮŪ╔½Ż¼ą╬│╔▓╗═¼Ą─ÖÓŽ▐ĘųŅÉŻ¼į┘īóĮŪ╔½Ęų┼õĮo▓╗═¼Ą─ė├æ¶Ż¼ą╬│╔▓╗═¼Ą─ė├æ¶╚║Ż¼Å─Č°▀_ĄĮ└ĒŽļĄ─ÖÓŽ▐┐žųŲą¦╣¹ĪŻ
ņ`╗ŅĄ─ŽĄĮy╣żŠ▀Ż║└¹ė├▀@ą®╣żŠ▀Ż¼ė├æ¶┐╔ęį▀MąąöĄō■éõĘ▌Īó▐DęŲ─ĻČ╚öĄō■ĪóÖz▓ķ║═ą▐š²öĄō■Īó╗“š▀ūįäė▀\ąąŅAČ©┴xĄ─öĄō■╠Ä└Ē▀^│╠ĪŻ
ŠÄ┤aČ©┴xŻ║═Ļ╚½ūįė╔Ą─ŠÄ┤aČ©┴x╣”─▄Ż¼ė├æ¶┐╔ęįČ©┴xŽĄĮyųą╩╣ė├Ą─▓┐ķTŠÄ┤aĪó╚╦åTŠÄ┤aĄ╚Ż¼▓óŪę┐╔ęį═©▀^ŠÄ┤aĄ─īė┤╬ĮYśŗūįäėą╬│╔┘Yį┤╣▄└ĒŲ„╩ĮĄ──┐õøśõĪŻ
╣żū„┴„╣żŠ▀Ż║śIäš┴„│╠┐╔ęį═©▀^łDą╬╗»Ą─╣żŠ▀įOų├Ż¼ĘĮ▒ŃČ©ųŲ║═ą▐Ė─ĪŻÅ─Č°▀_ĄĮĘĮ▒ŃĪó┐ņĮ▌Ą─śIäš╠Ä└Ēą¦╣¹Ż¼╠ßĖ▀╣żū„ą¦┬╩ĪŻ
Ė„ĘNśIäšå╬ō■Ą─┴„▐D▀^│╠Č╝Š▀ėąŲõ╠ž╩Ōų«╠ÄĪŻ╣żū„┴„╣▄└ĒŠ═╩Ū×ķ┐ņ╦┘š{š¹╣żū„┴„│╠Č°įOų├Ą──ŻēKĪŻßśī”├┐ĘNśIäš┴„▐DŁh╣ØĄ─▓╗═¼ĪóĮŪ╔½Č©┴xĄ─▓╗═¼Ą╚Ż¼ŽĄĮy╣▄└ĒåT┐╔ęįČ©┴xŽÓĻPĄ─┴„│╠Ż¼į┌┴„│╠Č©┴xųą┐╔╚╬ęŌįOų├┴„│╠╣سcĪŻŲõ▓┘ū„ĘĮ╩Į×ķłDą╬╗»═Ž└ŁĘĮ╩ĮŻ¼▓┘ū„Įń├µ×ķWEBłDą╬╗»Įń├µŻ¼╝╚Č©╝┤ė├Ż¼¤oąĶ▄ø╝■ķ_░lĪŻ
ĘŪ¼Fł÷īŹĢr╣▄┐žŽĄĮyū„×ķŲ¾śIą┼Žó╗»ŽĄĮyĄ─ę╗▓┐ĘųŻ¼į┌īŹļH▀\ąą▀^│╠ųąŻ¼▒ž╚╗║═Ųõ╦¹Ą─▄ø╝■░l╔·öĄō■╗“śIäš╔ŽĄ─┬ōŽĄŻ¼Ė∙ō■╬ęéāį┌įOéõ╣▄└ĒŽĄĮyĒŚ─┐īŹ╩®ĘĮ├µĄ─Įø“ׯ¼ĘŪ¼Fł÷īŹĢr╣▄┐žŽĄĮyą┼Žó╗»ĒŚ─┐ų„ę¬ėąęįŽ┬ÄūéĆĮė┐┌┤µį┌ĪŻ║═¼FėąERP╗“╣╠Č©┘Y«a╣▄└ĒŽĄĮyĄ─öĄō■╝µ╚▌Ż╗ ┼cDCSīŹĢrĀŅæBÖz£yŽĄĮyĄ─µ£ĮėŻ╗┼cMES╔·«a▀\ąą╣▄└ĒŽĄĮyŅA┴¶Įė┐┌Ż╗┼cē║┴”╣▄Ą└╣▄└ĒŽĄĮyŅA┴¶Įė┐┌Ż╗┼cģf═¼▐k╣½▄ø╝■īÅ┼·┴„Ą─öĄō■╗ź═©ŅA┴¶Įė┐┌Ż╗
4. ą¦ęµĘų╬÷
ßt╦ÄŲ¾śIĄ─║╦ą─śIäš╩Ū╩▓├┤Ż¼Š═╩ŪGMPŻ¼GMP▀^▓╗┴╦Š═ę¬ĻPķTĪŻČ°Ūęć°╝ęī”┤╦╩Ūėą├„┤_Ą─ĢrķgŽ▐ųŲĄ─Ż¼¤oŠ·ųŲä®2013─Ļ12į┬31╚šų«Ū░▀^▓╗┴╦Š═ĻPķTŻ╗Ųõ╦¹Ą─╣╠¾wųŲä®Īóę╗░ŃųŲä®2015─Ļ12į┬31╠¢ų«Ū░▀^▓╗┴╦ĻPķTĪŻī”┤╦Ż¼IT▓╗─▄ų├╔Ē╩┬═ŌŻ¼Č°╩Ūę¬│╔×ķ═Ļ│╔▀@ą®╣żū„Ą─╩ųČ╬║═╣żŠ▀ĪŻ╬ęéāć°╝ęĘŪ│Ż╝▒ė┌═©▀^GMPšJūCüĒ╠ßĖ▀╬ęéāć°╝ęĄ─ųŲ╦Äčbéõ╦«ŲĮ║═ųŲ╦Ä╦«ŲĮĪŻ
ć°ā╚Ą─╦ÄŲĘø]ėąĄ╚╝ēŻ¼ų╗ėą║ŽĖ±┼c▓╗║ŽĖ±ĪŻ╩ął÷╔ŽĄ─Å═ĘĮĄżģóŲ¼Ż¼▒Ńę╦Ą─╚²╬Õį¬ę╗Ų┐Ż¼┘FĄ─Č■╚²╩«į¬ę╗Ų┐Ż¼┘|┴┐╩Ū▓╗ę╗śėĄ─ĪŻūŅ▒Ńę╦Ą─Å═ĘĮĄżģóŲ¼Ż¼░┤ššć°╝ę╦ÄŲĘ╠ÄĘĮŻ¼▀BįŁ┴ŽĄ─ārĖ±Č╝ē“▓╗╔ŽĪŻ═¼śėŻ¼Ģ■ėąė├╠O╣¹Ųżū÷░Õ╦{Ė∙Ą─ĪŻ×ķ╩▓├┤ę¬▀@śėū÷Ż┐Š═╩Ūį┌╬ęéāć°╝ęŻ¼╦ÄĄĻĄ─Öz£yś╦£╩ų╗ĻPūó╗»īW│╔ĘųŻ¼▓╗ĻPūó╣ż╦ćĪŻų╗╦∙ęį╚ń┤╦Ż¼ę▓╩Ūę“×ķø]ėąŽÓæ¬Ą─öĄō■ū„ų¦ō╬ĪŻ
ą┬░µGMP║═ITų«ķgĄ─ĻPŽĄŻ¼╩Ūę¬═©▀^£p╔┘║═╚Ī┤·╚╦╣żĖ╔ŅAŻ¼üĒūŅ┤¾Ž▐Č╚ĄžĮĄĄ═╦ÄŲĘ┘|┴┐’LļUŻ¼╠ßĖ▀╦ÄŲĘ┘|┴┐ĪŻį┌ųŲ╦ÄŽĄĮyųąŻ¼╚╦╩ŪūŅ┤¾Ą─╬█╚Šį┤Ż¼Č°Ž¹│²▀@ę╗ę“╦žĄ─╬©ę╗┬ĘÅĮŻ¼Š═╩Ūūįäė╗»Īóą┼Žó╗»║═ųŪ─▄╗»Ż¼╚²╗»ų«╔ŽŻ¼ųžę¬Ą─╗∙ĄAŻ¼Š═╩ŪįOéõĄ─╝»│╔╗»ĪŻ╝»│╔╗»ū÷▓╗ĄĮŻ¼ūįäė╗»Īóą┼Žó╗»║═ųŪ─▄╗»ę▓¤oĘ©īŹ¼FĪŻą┬└ŽGMPėą▀@├┤ÄūéĆ▓╗═¼Ż║’LļUįu╣└ĪóŲ½▓ŅĘų╬÷║═“×ūCŻ¼▀@╚²éĆČ╝║═╬ęéā╦ÄŲĘ╔·«a¼Fł÷Ą─öĄō■▓╔╝»├▄ŪąŽÓĻPĪŻ
’LļUįu╣└┐┐╩▓├┤Ż┐┐┐öĄō■Ż¼┐┐¼Fł÷Ą─╣ż╦ćöĄō■Ż╗Ų½▓ŅĘų╬÷┐┐╩▓├┤Ż¼┐┐¼Fł÷▓╔╝»Ą─öĄō■Ż╗“×ūC┐┐╩▓├┤Ż¼┐┐¼Fł÷▓╔╝»Ą─öĄō■ĪŻ╦∙ęįą┬░µGMPĄ─║╦ą─╦╝Žļ║═ūŅ’@ų°Ą─Ė─▀MŻ¼┼cIT├▄ŪąŽÓĻPŻ¼ø]ėąöĄō■▀@╚²éĆ╣żū„Ė∙▒Šū÷▓╗┴╦ĪŻ
╦ÄŲĘ┘|┴┐’LļUĄ─╣▄└ĒŻ¼╩Ū╬ęéā╦ÄŲĘ╔·«a▀^│╠«öųąĘŪ│Żųžę¬Ą─Łh╣ØŻ¼ę¬ėąöĄō■ū÷ų¦ō╬Ż¼ø]ėąöĄō■Ą─įÆŻ¼’L┐žĖ∙▒Šū÷▓╗üĒĪŻ▀@╔µ╝░ĄĮę╗éĆ▒╚▌^īŻśIĄ─¢|╬„Ż¼Š═╩Ū’L┐žĄ─ā׎╚öĄŻ¼╩Ū═©▀^öĄō■Ą─ģ󚚯¼═©▀^Öz£yģóöĄüĒ▀Mąąš¹éĆ╦ÄŲĘ┘|┴┐’LļUĄ─╣▄└ĒĪŻęį¤oŠ·╔·«a×ķ└²Ż¼ŁhŠ│ģóöĄŻ¼įOéõ▀\ąąģóöĄŻ¼╣½ė├ŽĄĮyģóöĄČ╝┐╔─▄«a╔·Ų½▓ŅĪŻ┐┐╩ų╣ż╚źū÷Ų½▓ŅĘų╬÷Ż¼╩Ūę╗éĆĘŪ│ŻÅ═ļsĄ─▀^│╠Ż¼Č°ėŗ╦ŃÖCät╩ŪĘŪ│Ż║├Ą─▐kĘ©ĪŻ
╦ÄŲĘ╔·«aĄ─╚²┤¾ēKŻ¼ŁhŠ│ĪóįOéõĪó╣½ė├ą┼ŽóŽĄĮyŻ¼▀@╚²┤¾ēKČ╝ę¬═©▀^ę╗éĆķ_Ę┼Ą─öĄō■Įė┐┌Ż¼Ė·╣▄└ĒĪóįOéõ║═╣½ė├ą┼ŽóŽĄĮy▀MąąöĄō■Į╗ōQĪŻļŖūė┼·ėøõø¼Fį┌▀Ć▓╗×ķ╬ęéāć°╝ęĄ─╦Ä▒OŠųšJ┐╔Ż¼Ą½╩Ūį┌├└ć°FDAĄ─CGMP║═ÜW├└Ą─EUGMPųą╩ŪšJ┐╔Ą─ĪŻ
į┌GMPĖ─įņųąŻ¼╬ęéā═Č╚ļ┴╦┤¾┴┐Ą─┘YĮ║═Š½┴”ĪŻ×ķ╩▓├┤╚ń┤╦Ż¼Ą┌ę╗Ż¼ą┬░µGMPī”ė┌¤oŠ·╔·«aųŲ䮥─ŁhŠ│ėąį┌ŠĆ▒O£yĄ─ę¬Ū¾ĪŻĄ┌Č■╩Ū╦ÄŲĘ╔·«a┘|┴┐Ą─¼Fł÷▒O╣▄ĪŻę“×ķ¤oŠ·╔·«aŲ¾śIĄ─╠ž╩ŌąįŻ¼╔·«a▄ćķgĄ─¼Fł÷╣▄└ĒŠ═╩Ūę╗éĆ║┌Ž╗ūėŻ¼╚╦▓╗─▄ļS▒Ń▀M╚źĪŻ═©▀^į┌ŠĆ▒O£yŽĄĮyŻ¼Š═┐╔ęį░č║┌Ž╗ūėūā│╔ę╗éĆ═Ė├„Ą─¶~ĖūĪŻę╗Ą®░l¼F┴╦Ų½▓ŅŻ¼▀Ć┐╔ęįīŹĢr╝mŲ½Īóų╣ōpŻ¼▒▄├Ō│╔┼·╦ÄŲĘĄ─ł¾ÅUĪŻ
Ą┌╚²Ż¼Š═╩Ū╬ęéāć°╝ęĄ─╦ÄŲĘĘųĄ╚║═Ęų╝ēĪŻ¼Fį┌╦ÄŲĘĄ─▒O╣▄╩Ūęį╗»īWį¬╦žĄ─Ą╚═¼ąįüĒ▒O╣▄Ą─Ż¼ø]ėą┐╝æ]┼·┤╬╣ż╦ćĄ─ę╗ų┬ąįĪŻėą┴╦öĄō■ū÷ų¦ō╬Ż¼╬┤üĒŠ═┐╔ęį▀Mąą╦ÄŲĘ┘|┴┐Ą─ĘųĄ╚Ęų╝ēŻ¼šµš²īŹ¼F╦∙ų^Ą─ā×┘|ā×ārĪŻ
į┌¼Fį┌Ą─╝»ųą▓╔┘Å─Ż╩ĮŽ┬Ż¼ā×┘|ā×ārų╗╩Ūę╗éĆĖ┼─ŅŻ¼ø]ėą▐kĘ©┬õīŹĄĮ╬╗ĪŻšµš²īŹ¼Fā×┘|ā×ār▒žĒÜę¬░č╦ÄŲĘ╔·«aųŲįņ▀^│╠«öųąĄ─╣ż╦ćģóöĄ¾w¼F│÷üĒŻ¼▓┼Ģ■Ę┤ė│╦ÄŲĘĄ─┘|┴┐╠žš„Ż¼Č°▓╗āHāH╩Ū┐┤─ŃĄ─╗»īW│╔ĘųĪŻ▀@śėĄ─╣żū„Ż¼┐┐ę╗éĆ╦ÄÅS╩Ūū÷▓╗┴╦Ą─Ż¼▒žĒÜ┤¾╝ęę╗ŲüĒą╬│╔▀@śėę╗éĆĘšć·Ż¼ę¬Ū¾ć°╝ę║═š■Ė«üĒū÷▀@śėĄ─╩┬ŪķĪŻ
╬ęéāųŲ╦ÄŲ¾śIėąž¤╚╬üĒū÷▀@śėĄ─╩┬ŪķŻ¼│õĘų└¹ė├GMPĖ─įņĄ─ĢrÖCŻ¼═Ųäė▀@ę╗╣żū„ĪŻ┤¾öĄō■Ą─│┴ĄĒų╗╩ŪĮŌøQ┴╦öĄō■▓╔╝»Ą─å¢Ņ}Ż¼╬┤üĒ╬ęéāę¬ūīöĄō■šfįÆŻ¼īŹ¼F╦ÄŲĘĄ─┘|┴┐ĘųĄ╚Ęų╝ēŻ¼ęį╝░ųŲ╦Ä╣ż╦ćĄ─ā×╗»ĪŻųŲ╦Ä╣ż╦ćĄ─ā×╗»Ż¼ę¬ę└┐┐│╔─Ļ└█į┬╔·«aųŲįņ▀^│╠ųą│┴ĄĒŽ┬üĒĄ─öĄō■Ż¼▀@╩Ūī”ųŲ╦ÄŲ¾śIüĒšfŻ¼ĘŪ│Żųžę¬Ą─¢|╬„ĪŻ
Ą┌╦─╩Ū¼Fł÷┼Óė¢Ż¼ę“×ķį┌¤oŠ·ŁhŠ│Ž┬╔·«aĄ─åT╣żŻ¼ĘŪ│ŻąĶę¬ī”╦³¼Fł÷▓┘ū„▓╗ęÄĘČ║═Ų½▓Ņ¼Fł÷Į╠ė²Ą─┼Óė¢Ż¼═©▀^öĄō■Ą─▓╔╝»Ż¼░³└©ęĢŅlöĄō■▓╔╝»Ż¼┐╔ęįŠÄ│╔ę╗éĆ╗ŅĄ─Į╠▓─Ż¼ī”ė┌¤oŠ·ŁhŠ│Ž┬╔·«aĄ─╣”─▄ū÷¼Fł÷Ą─┼Óė¢ĪŻ
╦ÄŲĘ┘|┴┐╣▄└Ēėą╬Õ┤¾ę¬╦žŻ¼╚╦ĪóÖCĪó┴ŽĪóĘĄĪó▀ĆŻ¼░č▀@╬Õ┤¾ę¬╦ž┐žųŲūĪ┴╦Ż¼─ŃĄ─╦ÄŲĘ┘|┴┐Š═ėą▒ŻšŽ┴╦Ż¼▀@ę▓╩ŪGMPĄ─║╦ą─Ż¼GMPųvĄ─╩Ū╚½▀^│╠Ż¼╚½ĘĮ╬╗Ż¼╚½åTĄ─╣▄└ĒŻ¼╬Õ┤¾ę¬╦ž╚½▓┐┐žųŲūĪ┴╦Ż¼┘|┴┐╣▄└Ē▓┼šµš²ū÷ĄĮ╬╗┴╦ĪŻ┘|┴┐▓╗╩ŪÖz“×│÷üĒĄ─Ż¼Č°╩Ū╔·«a│÷üĒĄ─ĪŻ
╬ęéāę¬īŹ¼FĄ─╬Õ┤¾─┐ś╦Ż¼Ęųäe╩Ū╔·«a▀^│╠ę¬┐╔ęĢ╗»Ż¼įOéõ▀\ąąöĄūų╗»Ż¼╬’┴ŽŽ¹║─Š½╝Ü╗»Ż¼ŁhŠ│▒O┐žūįäė╗»Ż¼ą┼Žó╝»│╔ę╗¾w╗»Ż¼┐éĄ──┐Ą─Ż¼Š═╩ŪęįŪ░ųv▀^Ą─Ż¼ę¬Å─öĄō■╝ė╣ż│╔ą┼ŽóŻ¼Å─ą┼Žó╝ė╣ż│╔ų¬ūRŻ¼▀@╩Ūū÷ITČ╝ų¬Ą└Ą─╗∙▒ŠįŁ└ĒĪŻį┌ŠĆ▒O£yāHāHĮŌøQ┴╦öĄō■▓╔╝»Ą─å¢Ņ}Ż¼║¾├µūīöĄō■šfįÆŻ¼▀Ćėą║▄ķLę╗Č╬┬Ęę¬ū▀Ż¼æ¬įōėą║▄ČÓųŲ╦ÄŲ¾śIŻ¼░³└©ć°╦Ä▀@ą®┤¾Ų¾śIę╗Ųģó┼c▀MüĒŻ¼╠ßĖ▀╬ęéāć°╝ęĄ─ųŲ╦Ä╦«ŲĮĪŻ
▀@ę╗▌åą┬░µGMPĖ─įņŻ¼ļm╚╗ĄĮ12į┬31╠¢ęčĮøĮY╩°┴╦Ż¼Ą½╩Ū▀Ć┐╔ęį└^└m═∙Ž┬ū▀Ż¼ę╗░ŃųŲ䮥Į2015─Ļ▀Ćę¬ū▀Ż¼╬ęéā▓╗─▄į┘ū÷Ą═╦«ŲĮųžÅ═Į©įO▀@ę╗Śl└Ž┬Ę┴╦ĪŻ╝╚╚╗╗©┴╦ÕXŻ¼░┤ššÜW├└Ą─ś╦£╩ū÷┴╦ą┬░µĄ─GMPŻ¼Š═æ¬įōį┌įŁüĒĄ─╗∙ĄA╔Žį┘▀M▓Įę╗³cĪŻūįäė╗»Īóą┼Žó╗»║═ųŪ─▄╗»Ż¼╩Ūę╗Śl▒žė╔ų«┬ĘĪŻ
╦─ĪóŲ¾śIą┼Žó╗»╬┤üĒ░lš╣ęÄäØ
╣½╦Šīóė├2─ĻĄ─Ģrķg═Ļ│╔š¹¾w╔Ž╩ąŻ¼3─ĻĄ─Ģrķg╩╣╣½╦ŠĄ──Ļ«aųĄĄĮ▀_10éĆā|ęį╔ŽĪŻ5ų┴10─ĻĄ─Ģrķg░č╬õØhÉ█├±ųŲ╦ÄėąŽ▐╣½╦Š┤“įņ│╔ųąć°ę╗┴„Š▀ėąć°ļHŽ╚▀M╦«ŲĮĄ─ųŲ╦ÄŲ¾śIĪŻ
äóŽĒŲĮČŁ╩┬ķL╠ß│÷┴╦Į±─ĻĄ─╚²┤¾ųž³c╚╬䚯║1Īóį┌╣½╦Šīė├µ═Ųąą╚½├µĄ─ŅA╦Ń╣▄└ĒųŲČ╚Ż¼īŹ¼FõN╩█ŅA╦Ń→õN╩█─┐ś╦→õN╩█╣▄└ĒŻ╗2Īó▀Mąąęį─┐ś╦╣▄└Ē×ķįŁätĄ─┐āą¦┐╝║╦╣▄└ĒųŲČ╚Ą─ąĮ│ĻųŲČ╚Ė─Ė’Ż╗3Īó╚½├µ═Ųäė╣½╦ŠĄ─ą┼Žó╗»Į©įOŻ¼╔Ņ╗»║═öUš╣ ERPŽĄĮy║═OAŽĄĮyĄ─╩╣ė├Ż¼īŹ¼F╔╠śI┴„Ž“Ą─ą┼Žó╗»╣▄└ĒĪŻČ°─┐Ū░Ż¼╣½╦ŠāHāHīŹ¼F┴╦ERPųąĄ─╣®æ¬µ£╣▄└ĒŻ©×ķĮĄ¹K3ŽĄĮyŻ¼īŹļH╩╣ė├Ą──ŻēKāH║Ł╔w╗∙▒Šžöäš╣▄└Ē║═╬’┴Ž▓╔┘ÅĪóŅIė├Īó░lĘ┼╝░│╔ŲĘ│÷Äņ╣▄└ĒŻ®Ż¼OAŽĄĮyę▓ų╗īŹ¼F┴╦║åå╬Ą─Ó]╝■╩š░lĪó╬─╝■é„▀fĪóą┬┬äĪ󎹎ó╣▄└ĒĄ╚Ż¼─┐Ū░╣½╦ŠĄ─ą┼Žó╗»ĀŅørŻ¼ć└ųž▀mæ¬▓╗┴╦╣½╦ŠĄ─š¹¾w░lš╣ęÄäØĪŻ×ķ▀mæ¬╣½╦ŠĄ─┐ņ╦┘░lš╣Ż¼īŹ¼F┤“įņ│╔ųąć°ę╗┴„Š▀ėąć°ļHŽ╚▀M╦«ŲĮĄ─ųŲ╦ÄŲ¾śIĄ─║Ļéź─┐ś╦Ż¼ėą▒žę¬ī”╣½╦ŠĄ─ą┼Žó╗»Į©įOŻ¼▀Mąąą┬Ą─ęÄäØ║═öUš╣ĪŻ
ą┼ŽóŽĄĮyęÄäØ┐é¾w─┐ś╦Ż║ĮY║ŽÉ█├±Ą─Ė„ĒŚ╣▄└ĒųŲČ╚Ż¼Į©įOę╗╠ū║═É█├±░lš╣ŽÓŲź┼õĪó╗∙▒Š─▄ØMūŃÉ█├±╬┤üĒ3-5─Ļ░lš╣ąĶꬥ─ą┼Žó╗»╣▄└Ē║═ų¦ō╬ŲĮ┼_Ż¼Ę■äšė┌É█├±Ą─┐ņ╦┘░lš╣ĪŻ
▐D▌dšłūó├„│÷╠ÄŻ║═ž▓ĮERP┘YėŹŠWhttp://m.guhuozai8.cn/
▒Š╬─ś╦Ņ}Ż║¤oŠ·╔·«aį┌ŠĆ▒O£yŽĄĮy╠ß╔²╬õØhÉ█├±ųŲ╦Ä╣▄┐ž─▄┴”
▒Š╬─ŠWųĘŻ║http://m.guhuozai8.cn/html/consultation/10820617966.html